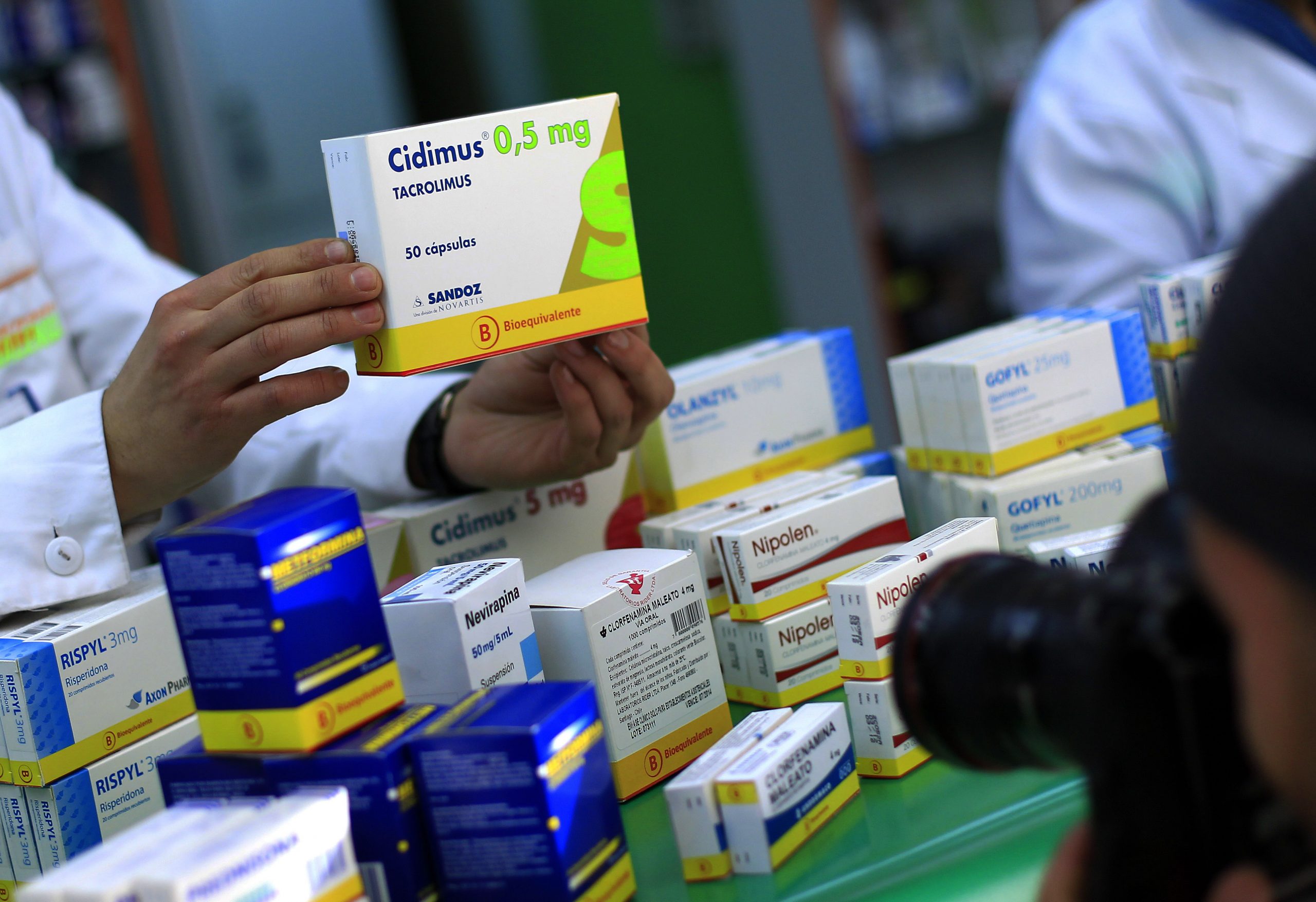
El Consejo para la Transparencia (CPLT) acogió el amparo de acceso a la información deducido en contra del Instituto de Salud Pública (IPS) y le ordenó proporcionar los antecedentes que permitieron al IPS inscribir en el Registro Sanitario el medicamento bioequivalente Sertralina Comprimidos 50 mg. elaborado por el Laboratorio Chile S.A.
La decisión del CPLT se adoptó luego que el Instituto no entregará los datos solicitados y le comunicará el requerimiento inicial de acceso a la farmacéutica que registro el fármaco, la cual se opuso a la entrega de cualquier tipo de información relacionada con la fórmula inscrita (en virtud del artículo 21 N°2 de la Ley de Transparencia), por tratarse de antecedentes confidenciales entregados al ISP con la finalidad exclusiva de obtener las autorizaciones sanitaria.
El medicamento Sertalina sostuvo el laboratorio es el resultado de una costosa y extensa investigación, y la divulgación de estos estudios al público implicaría afectar gravemente sus derechos comerciales y económicos. Añade que como entidad privada no le resulta aplicable el principio de transparencia de la Administración del Estado, además, resalta que su negativa de publicitar la información requerida se encuentra respaldada en los derechos fundamentales de propiedad y privacidad, pues se encuentra en peligro tanto su secreto empresarial (Know How de la compañía) como la confidencialidad empleada en el resguardo del producto. Por último, expone que el CPLT debe considerar el test de daños y de interés público para este caso, dado que este último no puede prevalecer sobre el legítimo interés y derechos de Laboratorio Chile de mantener en reserva tales antecedentes.
En el amparo de acceso a la información que fue acogido a trámite por el CPLT, el órgano requerido reiteró su negativa a proporcionar los estudios y resultados farmacéuticos del medicamento, en base a la causal de reserva prevista en el artículo 21 N°2 de la Ley de Transparencia, pues de entregarse la información solicitada se afectarían los derechos del tercero opositor.
Por su parte, Laboratorios Chile reiteró las implicancias negativas derivadas de la entrega de los antecedentes que obran en poder del Instituto Nacional de Salud, al tener las características de datos sensibles y reservados. Además, el reclamante no explicita los motivos de su petición (por qué considera relevante o necesario acceder a los antecedentes que la empresa le suministro a la administración). Por último, alega que el solicitante es una persona que ha presentado 69 amparos ante el CPLT (32 durante este año), demostrando una práctica habitual de efectuar solicitudes sin mayores fundamentos o sin estar asociada a un estudio o fin determinado, lo que pugna con el espíritu de la Ley de Transparencia.
El CPLT acogió el amparo de acceso a la información. En primer lugar descarta la alegación de falta de motivación del reclamante, al señalar que “(…) se debe hacer presente que el artículo 12 de la Ley de Transparencia, que regula las exigencias aplicables a una solicitud de acción a la información, no establece en caso alguno como requisito de procedencia de la petición el señalamiento de las razones o fundamentos de la solicitud, ni menos que se explique el uso que dará a los antecedentes que se requieren. Por lo anterior, dicho antecedente no puede constituirse en un fundamento válido para transformar a la información que obra en poder de un órgano del Estado en secreto o reservada, debiendo desestimarse las alegaciones fundadas en este aspecto”.
Enseguida, explica que los antecedentes solicitados obran en poder del Instituto y son públicos, esto con base en los artículos 96 inciso primero del Código Sanitario, y 18 inciso primero y 20 del DS N°3 de 2010 del Minsal, “(…) por cuanto se trata de documentos que sirvieron de fundamento al ISP para autorizar el registro del medicamento consultado, los cuales se encuentran en posesión del reclamado, en virtud de las facultades otorgadas a éste, entre otros, por el citado artículo 96 del Código Sanitario, y forman parte de los procedimientos que utilizó el Instituto para ordenar la inscripción del producto farmacéutico en cuestión en el registro sanitario, autorizando, por tanto, su distribución o utilización a cualquier título en el territorio nacional, según prescribe el artículo 20 del citado Reglamento”. Ello, permite desestimar las alegaciones efectuadas por el tercero interesado, referidas a que los antecedentes solicitados se encontrarían excluidos de las obligaciones de transparencia que pesan sobre los organismos públicos y que tendrían el carácter de secretos.
A continuación, señala que el medicamento bioequivalente no goza del mismo resguardo intelectual/industrial que un producto inédito, de acuerdo a los artículos 89 y 90 de la Ley 19.039, sobre Propiedad Intelectual, en concordancia con el artículo 5 N°25 del Reglamento de Productos Farmacéuticos. Al efecto señala, que “(…) atendido que lo consultado dice relación con los estudios presentados para la aprobación de un fármaco bioequivalente, y no de una nueva entidad química, dicho antecedente se encuentra excluido de reserva legal”.
Bajo esta misma línea argumentativa, explica que el CPLT ha cambiado su anterior postura (Roles N°s C3301-20, C5023-20, C6200-20 Y C755-22) respecto a la reserva de los antecedentes relativos a la fórmula de productos farmacéuticos, considerando actualmente (mediante los Roles N°s C754-22 y C748-22) que por su naturaleza los productos farmacéuticos catalogados como bioequivalentes o equivalentes terapéuticos no constituyen una nueva entidad química y, en consecuencia, no son productos innovadores, pues se refieren a medicamentos que ya ha sido previamente registrados ante la autoridad competente.
En definitiva, el CPLT resuelve que “(…) en adecuación al concepto de interés público precedentemente, identificado con el beneficio superior de la sociedad globalmente considerada como un todo, la divulgación de los antecedentes consultados permitiría, a juicio de esta Corporación, fortalecer la confianza pública de la ciudadanía en la utilización de medicamentos bioequivalentes, cuya publicidad permite la comparación con los componentes autorizados para los fármacos originales, incidiendo directamente en el fortalecimiento de la confianza pública en el acceso a medicamentos de menor costo, otorgando así un mayor tranquilidad y confianza en relación a la utilización de dichos medicamentos; ello, en pos del interés nacional y de la salud pública, así como del derecho a la integridad física y psíquica de las personas consagradas en el artículo 19 N°1 de la Constitución”.
El CPLT desestimó las alegaciones del Laboratorio Chile y del ISP, acogió el amparo y ordenó la entrega de los estudios requeridos.
Vea decisión del Consejo para la Transparencia Rol N°C749-22.